6g xhttps://bgk-photo.cdn.bcebos.com/8694a4c27d1ed21bcc741a85bd6eddc451da3f14.jpgx=7.1g答:至少需要氯气的质量7.1g.故答案为:(1)2HCl CuOhttps://bgk-photo.cdn.bcebos.com/dcc451da81cb39db7f7d5336c0160924ab183014.jpgCuCl2 H2O;(2)置换反应;(3)7.1g.(2016江苏省南京市)21.图中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的.在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质,其中G为紫红色固体,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能;B可用来改良酸性土壤;A,F均为由三种元素组成的盐.图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.(1)写出化学式:G Cu ;(2)写出A与C反应的化学方程式 Na2CO3 H2SO4=Na2SO4 H2O CO2↑ ;写出D与E反应的化学方程式 CuO H2https://bgk-photo.cdn.bcebos.com/9358d109b3de9c8247c6cdef7c81800a19d8432a.jpgCu H2O ;写出H→I反应的化学方程式 Al 3AgNO3═Al(NO3)3 3Ag .https://bgk-photo.cdn.bcebos.com/838ba61ea8d3fd1fe3aa965a204e251f95ca5f2a.jpg
6g xhttps://bgk-photo.cdn.bcebos.com/8694a4c27d1ed21bcc741a85bd6eddc451da3f14.jpgx=7.1g答:至少需要氯气的质量7.1g.故答案为:(1)2HCl CuOhttps://bgk-photo.cdn.bcebos.com/dcc451da81cb39db7f7d5336c0160924ab183014.jpgCuCl2 H2O;(2)置换反应;(3)7.1g.(2016江苏省南京市)21.图中A~I是初中化学常见的物质,且分别是由H、
C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的.在通常情况下,D与其他物质的状态不同,
D、G、H、I均为单质,其中G为紫红色固体,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能;B可用来改良酸性土壤;A,F均为由三种元素组成的盐.图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.(1)写出化学式:G Cu ;(2)写出A与C反应的化学方程式 Na2CO3 H2SO4=Na2SO4 H2O CO2↑ ;写出D与E反应的化学方程式 CuO H2https://bgk-photo.cdn.bcebos.com/9358d109b3de9c8247c6cdef7c81800a19d8432a.jpgCu H2O ;写出H→I反应的化学方程式 Al 3AgNO3═Al(NO3)3 3Ag .https://bgk-photo.cdn.bcebos.com/838ba61ea8d3fd1fe3aa965a204e251f95ca5f2a.jpg
发布时间:2025-03-12 00:20:38
 Cu H2O;H→I反应,即铝与硝酸银溶液反应生成硝酸铝溶液和银,反应的化学方程式为:Al 3AgNO3═Al(NO3)3 3Ag.故答案为:(1)Cu;(2)Na2CO3 H2SO4=Na2SO4 H2O CO2↑;CuO H2
Cu H2O;H→I反应,即铝与硝酸银溶液反应生成硝酸铝溶液和银,反应的化学方程式为:Al 3AgNO3═Al(NO3)3 3Ag.故答案为:(1)Cu;(2)Na2CO3 H2SO4=Na2SO4 H2O CO2↑;CuO H2 Cu H2O;Al 3AgNO3═Al(NO3)3 3Ag.(2016江苏省南京市)22.空气中氧气含量测定的再认识.【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有 BCD .A.实验过程中没有污染B.在汞槽中起到液封作用C.生成的化合物加热分解又能得到汞和氧气D.能将密闭装置内空气中的氧气集合耗尽【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式 4P 5O2
Cu H2O;Al 3AgNO3═Al(NO3)3 3Ag.(2016江苏省南京市)22.空气中氧气含量测定的再认识.【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有 BCD .A.实验过程中没有污染B.在汞槽中起到液封作用C.生成的化合物加热分解又能得到汞和氧气D.能将密闭装置内空气中的氧气集合耗尽【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式 4P 5O2 2P2O5 .兴趣小组用该方法测出的氧气含量常常远低于21%.【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?【进行猜想】(1)装置漏气;(2) 红磷不足 装置内氧气有剩余;…【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因 白磷的着火点比红磷的着火点低 .【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因: 装置内残留的氧气更少,实验结果更准确 .【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氧化钠等物质又进行了实验(装置如图4),8分钟后测得的数据如表:实验前的体积 实验后的体积集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水131mL 90.0mL 63.6mL请计算出空气中氧气含量 20.2% (计算结果保留一位小数)【结论与反思】通过上述实验探究,选择 铁粉、炭粉、氧化钠和蒸馏水 (填物质名称)进行实验,可较为快速地完成实验并减小实验误差.【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由. 不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽
2P2O5 .兴趣小组用该方法测出的氧气含量常常远低于21%.【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?【进行猜想】(1)装置漏气;(2) 红磷不足 装置内氧气有剩余;…【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因 白磷的着火点比红磷的着火点低 .【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因: 装置内残留的氧气更少,实验结果更准确 .【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氧化钠等物质又进行了实验(装置如图4),8分钟后测得的数据如表:实验前的体积 实验后的体积集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水131mL 90.0mL 63.6mL请计算出空气中氧气含量 20.2% (计算结果保留一位小数)【结论与反思】通过上述实验探究,选择 铁粉、炭粉、氧化钠和蒸馏水 (填物质名称)进行实验,可较为快速地完成实验并减小实验误差.【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由. 不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽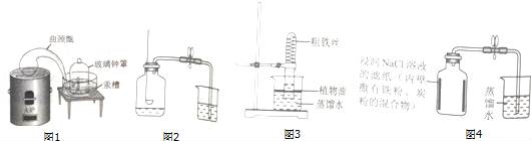 解:【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有在汞槽中起到液封作用;生成的化合物加热分解又能得到汞和氧气;能将密闭装置内空气中的氧气集合耗尽,故选BCD;【实验回顾】磷和氧气在点燃的条件下生成五氧化二磷,反应的化学方程式为:4P 5O2
解:【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有在汞槽中起到液封作用;生成的化合物加热分解又能得到汞和氧气;能将密闭装置内空气中的氧气集合耗尽,故选BCD;【实验回顾】磷和氧气在点燃的条件下生成五氧化二磷,反应的化学方程式为:4P 5O2 2P2O5;【进行猜想】实验中所取的红磷不足(或实验前没有夹弹簧夹、实验装置可能未冷却就打开弹簧夹等);【实验与交流】小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低;【交流与反思】铁丝在水、氧气的条件下很容易生锈,与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:装置内残留的氧气更少,实验结果更准确;【实验探究2】烧杯内蒸馏水减少的体积为氧气的体积=90mL﹣63.6mL=26.4mL空气中氧气含量=
2P2O5;【进行猜想】实验中所取的红磷不足(或实验前没有夹弹簧夹、实验装置可能未冷却就打开弹簧夹等);【实验与交流】小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低;【交流与反思】铁丝在水、氧气的条件下很容易生锈,与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:装置内残留的氧气更少,实验结果更准确;【实验探究2】烧杯内蒸馏水减少的体积为氧气的体积=90mL﹣63.6mL=26.4mL空气中氧气含量=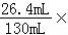 100%≈20.2%【结论与反思】通过上述实验探究,选择铁粉、炭粉、氧化钠和蒸馏水或白磷等物质进行实验,可较为快速地完成实验并减小实验误差.【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,不能比较准确地测定空气中氧气的含量,因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.【经典赏析】BCD.【实验回顾】4P 5O2
100%≈20.2%【结论与反思】通过上述实验探究,选择铁粉、炭粉、氧化钠和蒸馏水或白磷等物质进行实验,可较为快速地完成实验并减小实验误差.【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,不能比较准确地测定空气中氧气的含量,因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.【经典赏析】BCD.【实验回顾】4P 5O2 2P2O5;【进行猜想】红磷不足;【实验与交流】白磷的着火点比红磷的着火点低;【交流与反思】装置内残留的氧气更少,实验结果更准确;【实验探究2】20.2%;【结论与反思】铁粉、炭粉、氧化钠和蒸馏水;【拓展延伸】不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.
2P2O5;【进行猜想】红磷不足;【实验与交流】白磷的着火点比红磷的着火点低;【交流与反思】装置内残留的氧气更少,实验结果更准确;【实验探究2】20.2%;【结论与反思】铁粉、炭粉、氧化钠和蒸馏水;【拓展延伸】不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.

