38.4gCu跟适量的浓HNO3反应,Cu全部作用后,在标准状况下收集到气体22.4L,求消耗的HNO3的物质的量是多少?
38.4gCu跟适量的浓HNO3反应,Cu全部作用后,在标准状况下收集到气体22.4L,求消耗的HNO3的物质的量是多少?
发布时间:2025-03-04 09:41:20
38.4gCu跟适量的浓HNO3反应,Cu全部作用后,在标准状况下收集到气体22.4L,求消耗的HNO3的物质的量是多少?
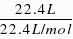 =1 mol,无论生成NO2还是NO,生成一个气体分子需要一个硝酸分子参加氧化还原反应,根据氮原子守恒得参加氧化还原反应的硝酸的物质的量为n(HNO3)=n(NO2) n(NO)=1 mol;铜和硝酸反应生成硝酸铜,根据铜原子守恒得n(Cu)=n(Cu(NO3)2)=
=1 mol,无论生成NO2还是NO,生成一个气体分子需要一个硝酸分子参加氧化还原反应,根据氮原子守恒得参加氧化还原反应的硝酸的物质的量为n(HNO3)=n(NO2) n(NO)=1 mol;铜和硝酸反应生成硝酸铜,根据铜原子守恒得n(Cu)=n(Cu(NO3)2)=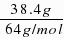 =0.6mol,根据硝酸铜的化学式知,起酸作用的硝酸是铜的物质的量的2倍,所以可知表现酸性的硝酸的物质的量为0.6×2=1.2 mol,所以参加反应的硝酸的物质的量为:1mol 1.2mol=2.2mol.答:消耗的HNO3的物质的量是2.2mol.
=0.6mol,根据硝酸铜的化学式知,起酸作用的硝酸是铜的物质的量的2倍,所以可知表现酸性的硝酸的物质的量为0.6×2=1.2 mol,所以参加反应的硝酸的物质的量为:1mol 1.2mol=2.2mol.答:消耗的HNO3的物质的量是2.2mol.
